Сложная хирургия рака поджелудочной железы и полная регрессия сердечной недостаточности
«Чего вы хотели? Это же рак. Тем более, поджелудочной железы. Они вам в Москве рассказали, что это можно лечить, а на самом деле все плохо. Что ни делай, ничего не поможет». И этот текст сопровождается соответствующими действиями, точнее их отсутствием.
Хирургия местнораспространенного рака поджелудочной железы и полная регрессия сердечной недостаточности у пациента с инфарктом и гибернацией половины миокарда
Что может выпасть на долю пациента, насколько важны для него близкие люди и насколько опасно безразличные, в этой статье. Это история о том, какие проблемы могут возникнуть после аутотрансплантации тонкой кишки даже после выписки и почему пациенту нужно держать связь с оперирующим хирургом и лечащим врачом.
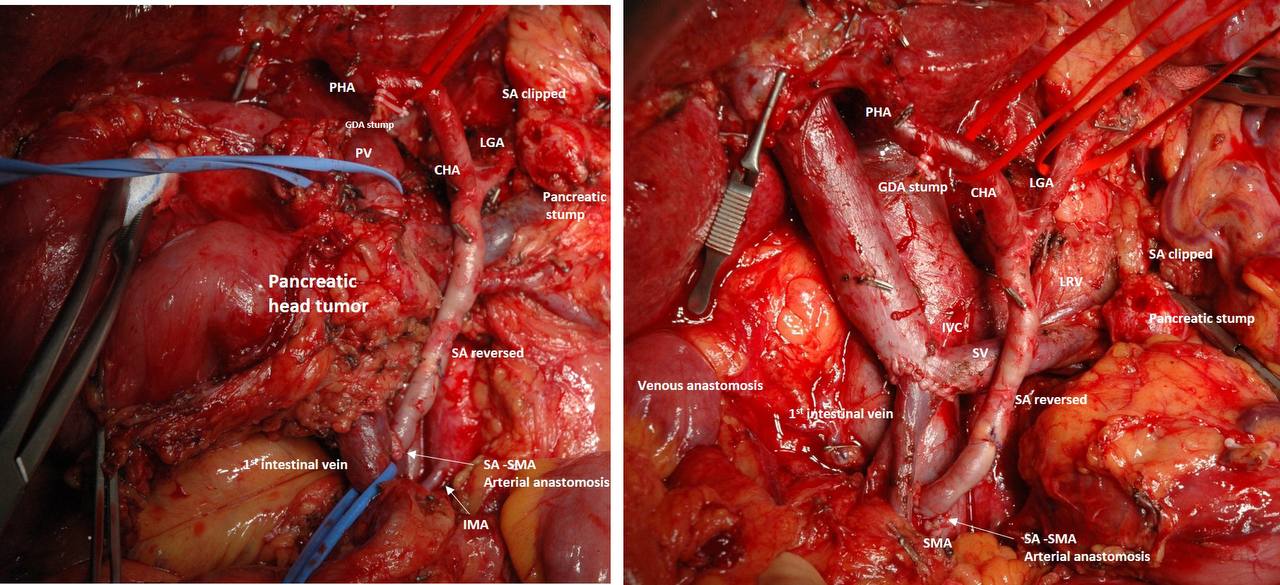
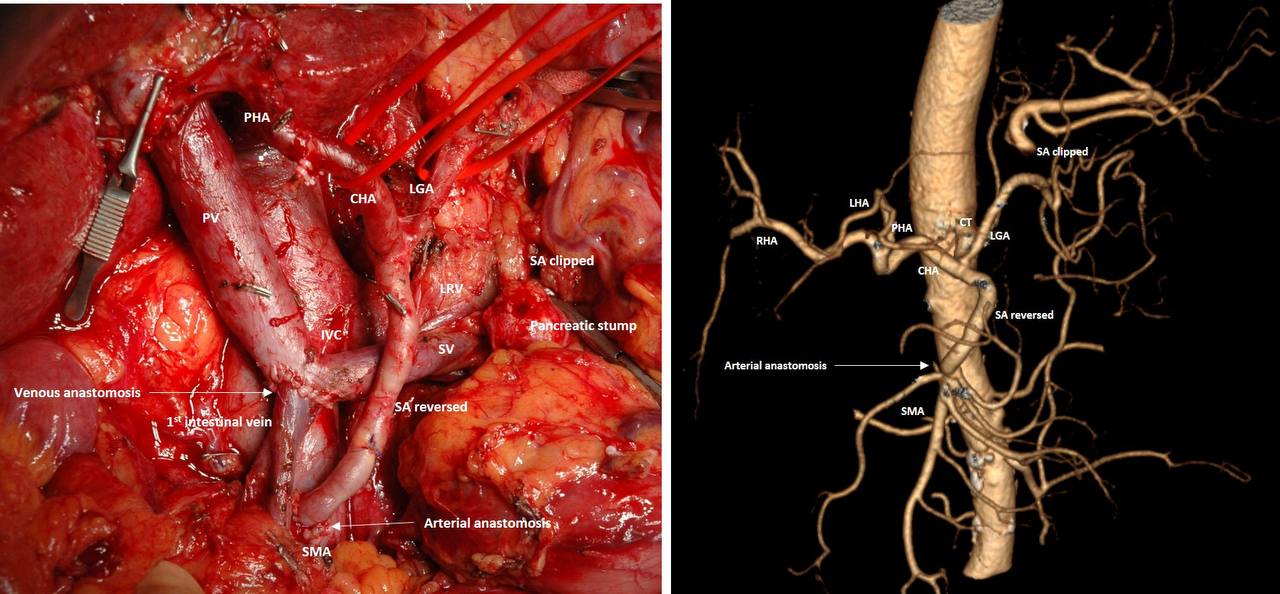
Операция: Панкреатодуоденальная резекция, резекция корня брыжейки тонкой кишки, резекция селезеночной и верхней брыжеечной артерии (ВБА) со сплено-верхнебрыжеечным анастомозом с дистальным отрезком ВБА, резекция верхней брыжеечной вены (ВБВ) и всех ее притоков с анастомозом ВБВ с 1-ой тонкокишечной веной (аутотрансплантация тонкой кишки). Атипическая резекция желудка. Методика «Arterial resection and reconstruction first, R0-pancreatectomy and vein resection second»
Pylorus- preserving Whipple + SMA and SMV (with all the tributaries) resection, resection of the root of mesentery and splenic artery, spleno-SMA anastomosis, SMV-1-st mesenteric vein anastomosis (intestinal autoTx). Ductal adenocarcinoma, усT4NхM0, yp T4 N2(52/0), Pn1,L0, V1, A1, R0.
Четыре месяца назад, через 12 дней после радикальной операции мы выписали пациента 64 лет с диагнозом: Высокодифференцированная протоковая аденокарцинома головки поджелудочной железы, усT4NхM0, yp T4 N0(52/0), Pn1, V1, A1, L0, R0 с умеренно выраженным ответом на проведенную терапию (12 курсов неоадъювантной химиотерапии FOLFIRINOXом)-Tumor Regression Score 2 (mRyan R, CAP Protocol). Гастроинтестинальная стромальная опухоль желудка.
Ductal adenocarcinoma of the pancreatic head and body, G1, with invasion of the duodenum, peripancreatic soft tissue, invasion of the SMA and SMV (with all its tributaries). Moderate but defined treatment response after FOLFIRINOX (12) – TRS 2 (mRyan R, CAP Protocol). Gastric GIST.
При первичном КТ был выявлен рак крючковидного отростка ПЖ с прорастанием 12-перстной кишки и циркулярным контактом с ВБА и ВБВ на протяжении более 4-5 см без отдаленных метастазов. Согласно рекомендациям, при местнораспространенном раке ПЖ была назначена предоперационная химиотерапия. После 12-ти курсов FOLFIRINOXа, опухоль уменьшилась в размерах, но сохранялся циркулярный контакт с ВБА на протяжении около 4 см и с ВБВ почти на всем её протяжении, с вовлечением всех ее притоков. При этом варикозных вен не было обнаружено.
Контрольные КТ, МРТ и ПЭТ/КТ не выявили отдаленных метастазов. Онкомаркер СА 19-9 за это время снизился с 670 до 91 ед./ мл. Возможности лучевой терапии в этом случае (и обычно при этой локализации опухоли) ограничены в связи с вовлечением такого критического органа, как 12-перстная кишка. Ситуация интенсивно и неоднократно обсуждалась на онконсилиумах, с пациентом, его женой и дочерями.
Принимая во внимание то, что резектабельность опухоли, определяемая с помощью КТ, МРТ или ПЭТ/КТ после неоадъювантного лечения местнораспространенных и погранично-резектабельных опухолей, ненадежна (NCCN, PANC-A), отсутствие прогрессирования во время и после неоадъювантной химиотерапии, отличный физически статус (ECOG 0), в соответствии с рекомендациями NCCN, PANC 5, было решено предпринять попытку выполнения радикальной (R0) резекции ПЖ с резекцией вовлеченных в опухоль артерий и вен. Операцию удалось выполнить в радикальном объеме, хвост железы и селезенка с селезеночной веной были сохранены, несмотря на то, что селезеночная артерия была резецирована, а ее проксимальная часть реверсирована и анастомозирована с дистальной непораженной частью ВБА (артериальный анастомоз выполнил Сослан Дзигасов). Артериальный кровоток в селезенку обеспечили коллатерали из левой желудочной артерии.
Единственным венозным притоком, подходящим для анастомозирования со стволом ВБВ, была 1-ая тонкокишечная вена (окклюзированная, но без вовлечения в опухоль). Находкой оказалась гастроинтестинальная опухоль желудка (вид саркомы) диаметром 2 см которая также была удалена. Послеоперационный период без осложнений, выписан домой с дренажом, по которому отделялось 400 мл серозной жидкости.
По прибытии домой в известный курортный город три дня всё шло отлично, но на четвертый по дренажу появилось до 2 литров отделяемого белого цвета (это лимфорея – истечение лимфы, насыщенной жиром, всасывающимся из кишки, т.к. брыжейка тонкой кишки была полностью пересечена при аутотрансплантации, лимфатические сосуды были либо клипированы, либо перевязаны. После операции может происходить прорезывание нити или соскальзывание клипсы, и лимфа начинает поступать в брюшную полость, что и случилось у нашего пациента). Такое отделяемое сохранялось 3-4 дня и привело к серьезному обезвоживанию. На фоне развившейся слабости он перестал вставать и стал меньше есть и пить, из-за чего слабость прогрессировала.
Обеспокоенные родственники обращались к врачам, но, несмотря на подробную информацию из выписки, те, к сожалению, давали типичные ответы: «Чего вы хотели? Это же рак. Тем более поджелудочной железы. Они вам в Москве рассказали всякого, а на самом деле все плохо. Что ни делай, ничего не поможет». И этот текст сопровождался соответствующими действиями, точнее их отсутствием, хотя даже внутривенное восполнение потерянного объема жидкости могло бы значимо помочь пациенту.
Родственники решились на отчаянный шаг, и из местной больницы реанимобилем (за 21 час) пациент в тяжелом состоянии с выраженными водно-электролитными и белковыми нарушениями, почечной и дыхательной недостаточностью был доставлен в реанимацию Ильинской больницы.
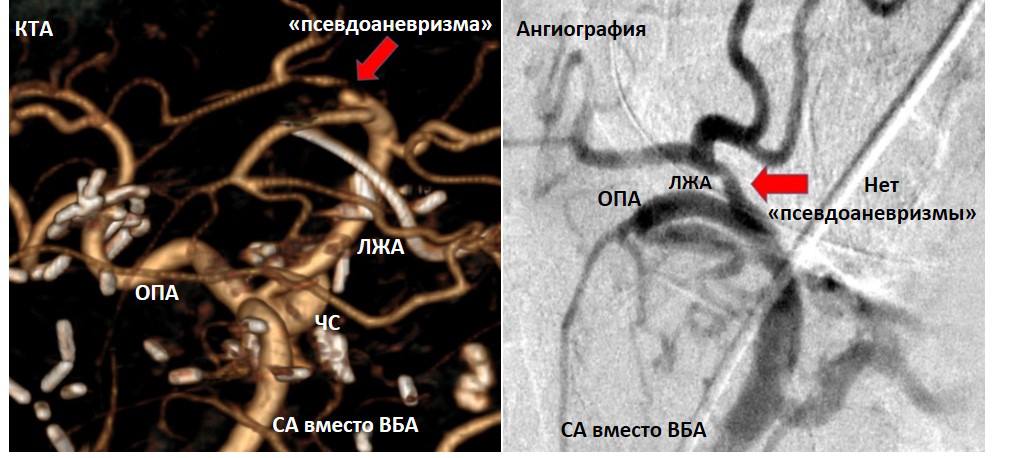
В день поступления на КТ была выявлена псевдоаневризма одной из ветвей левой желудочной артерии (см. КТ-ангиограмму, КТА), а это предшественник разрыва артерии и тяжелого кровотечения. Экстренно выполнена селективная ангиография. Подозрения не подтвердились: при сравнении ангиограмм и КТА это расхождение данных расценено как локальная отслойка интимы (внутреннего слоя артериальной стенки) с формированием слепого затека крови, имитировавшая "псевдоаневризму" на КТ, которая к моменту проведения селективной ангиографии затромбировалась. Из живота было удалено около 700 мл серозной жидкости: посев роста не дал, при цитологии опухолевых клеток не обнаружено.
На следующий день пациент стал жаловаться на слабость, на ЭКГ - подъем сегмента ST практически во всех грудных отведениях и высокий тропонин крови (1,598 нг\мл). Ситуация расценена как инфаркт миокарда (STEMI), проведена транслюминальная баллонная ангиопластика со стентированием передней межжелудочковой артерии в экстренном порядке (два лекарственно-покрытых стента).
При ЭХО КГ: выраженные нарушения локальной сократимости левого желудочка – акинез (отсутствие движений) верхушки и средних сегментов передней стенки и перегородки, с распространением на боковую стенку сердца. Глобальная сократимость левого желудочка снизилась вдвое (!): фракция выброса - 31%, выпот в полости перикарда - 200 мл. Признаки объемной перегрузки правых отделов. Ночью развилась острая левожелудочковая недостаточность с отеком легких (Killip 3), которая была купирована. Водно-электролитные нарушения и алиментарная недостаточность постепенно купировались, и прогноз стал определяться заболеванием сердца, развившегося, видимо, на фоне вышеуказанных метаболических нарушений. Продолжены мероприятия, направленные на компенсацию белковой недостаточности и плавное снижение преднагрузки инициацией диуреза (петлевые диуретики титровались под контролем электролитов плазмы).
Через трое суток начата реабилитация после инфаркта миокарда на фоне сложной и постоянно меняющейся кардиальной терапии. Холтеровский мониторинг не выявил нарушений ритма. Через 12 дней при ЭХО КГ отмечен рост фракции выброса до 40%, спустя еще семь дней – до 53%.
Акинеа и гипокинез исчезли, что заставило нас усомниться в ранее уставленном диагнозе инфаркта миокарда (ИМ). Предположен синдром Такоцубо, наличие которого потребовало бы корректировки лечения. Спустя 35 суток после развития ИМ для верификации диагноза мы провели МРТ сердца с гадолинием: в миокарде левого желудочка (ЛЖ) в передне-перегородочной области на границе среднего и базального сегментов определена небольшая зона субэндокардиального накопления контраста (около 30% от толщины миокарда), максимальным размером до 9 мм. Других значимых изменений миокарда не получено. Таким образом, ранее установленный диагноз «передне-перегородочный и верхушечнный инфаркт миокарда с распространением на боковую стенку, с подъемом сегмента ST» был подтвержден, однако объем необратимого повреждения миокарда оказался многократно меньше предполагаемого.
Длительный акинез участков миокарда и его последующая полная регрессия были расценены как «гибернация» миокарда на фоне тяжелых белково-энергетических и водно-электролитных расстройств. По мере их компенсации и терапии сердечной недостаточности (в т.ч. вовремя выполненной реваскуляризации) мышца сердца полностью восстановила свою сократительную способность, сформировавшаяся зона некроза оказалась минимальной и не определяет более прогноз пациента.
Благодаря лечению и заботе близких состояние нашего пациента (он вернулся к своему обычному образу жизни), позволило нам выписать его в родной город с обещанием с его стороны быть с нами в постоянном контакте, в том числе учитывая особенности отечественного государственного здравоохранения.
На фото: операция, ее конечный результат, КТ после 12 курсов ХТ, эхо КГ с гибернацией миокарда и полным восстановлением сократимости, «псевдопсевдоаневризма» левой желудочной артерии – загадочная история, которую полезно иметь в виду.
Кардиологи: Щекочихин Д.Ю., Гришковец А.И., Шорников С.Б.
Лучевая диагностика: Попов П.А., Амосова Е.Л., Кондратьев Е.В., Рыкова С.Ю., Амяга А.В., Харечко С.Г.
Ангиоваскулярный хирург: Терехин С.А.






 Егоров Вячеслав Иванович
Егоров Вячеслав Иванович