Руководитель отделения гинекологии и онкогинекологии Ильинской больницы, онкогинеколог-хирург, к.м.н. Антон Алексеевич Ильин совместно с партнерами 9 декабря провел конференцию с международным участием, на которой специалисты обсудили самые актуальные вопросы лечения онкогинекологических заболеваний.
Спикерами выступили специалисты из ведущих клиник и институтов США и Европы, таких как Cedars-Sinai Medical Center (Беверли-Хиллз, Калифорния, США), Медицинский центр им. Х.Шиба (Тель-Авив, Израиль), Йельский университет (Нью-Хейвен, Коннектикут, США), Европейский институт онкологии (Милан, Италия), Лондонский университет (Лондон, Великобритания), а также эксперты из крупных клиник и Федеральных центров России.
Видеозапись конференции со всеми докладами
Ниже представлены основные выводы по некоторым выступлениям.
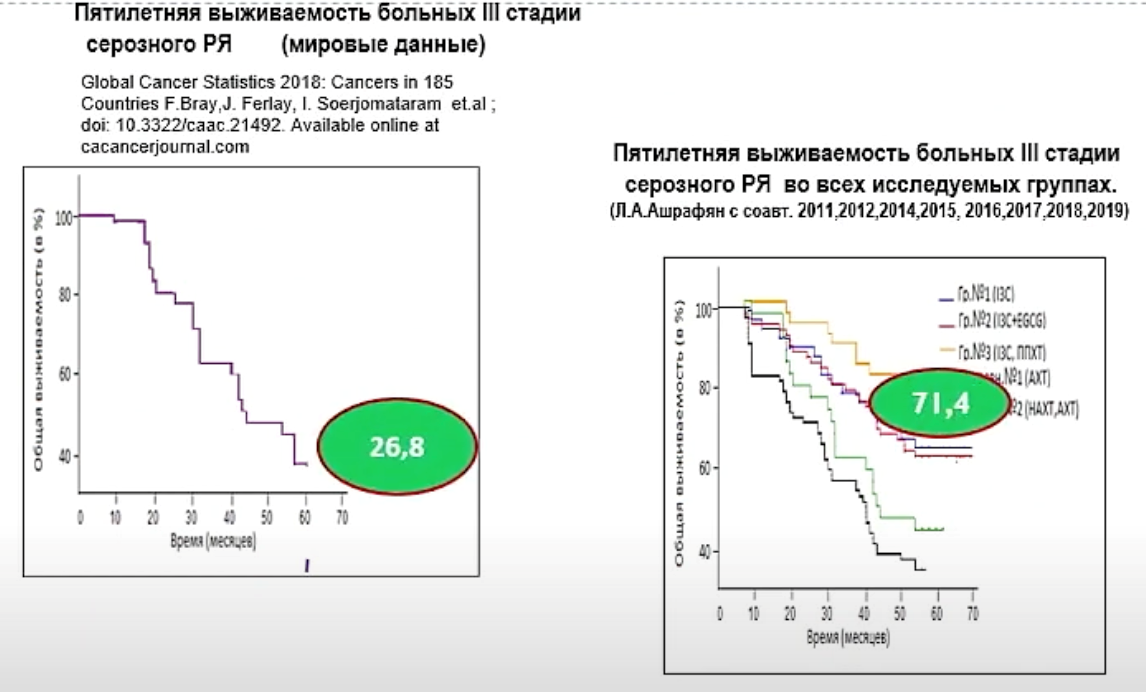
“Рак яичников: концепция патогенеза и принципы эффективной терапии”, Ашрафян Лев Андреевич, Академик РАН, д.м.н., профессор, заместитель директора ФГБУ НМИЦ АГП ИМ. В.И. КУЛАКОВА, директор института онкогинекологии и маммологии, Москва, Россия.
Лев Андреевич рассказал про влияние микроокружения опухоли и цитокиного профиля на эффективность лечения рака яичников: добавление Промисана увеличивает общую пятилетнюю выживаемость при раке яичников с 26% до 71%.
"Менопаузальная гормональная терапия в онкогинекологии. За и против", Ульрих Елена Александровна, д.м.н., профессор, главный научный сотрудник научно-исследовательской лаборатории репродуктивных технологий, руководитель центра компетенций «Онкофертильность» НМИЦ им. В. А. Алмазова, Санкт-Петербург, Россия.
Менопаузальная гормональная терапия (МГТ) в онкогинекологии всегда была спорной темой, учитывая, что значительная часть опухолей женской репродуктивной системы гормонозависимы. Однако в последние годы показания к МГТ расширяются. Елена Александровна рассказала, в каких случаях назначение гормонов с целью коррекции симптомов климакса безопасно, а в каких этого делать не стоит.
“Unresolved issues in sexual disfunction treatment after specialized treatment in oncogynaecology” (“Нерешенные проблемы лечения сексуальной дисфункции в онкогинекологии”), Alexandra Dubinskaya, MD, PhD, Cedars-Sinai Medical Center, Беверли-Хиллз, Калифорния, США.
Качество жизни пациентов после лечения рака женских половых органов страдает в наибольшей степени по сравнению с опухолями иных локализаций. Александра Дубинская рассказала о влиянии специализированного лечения на качество сексуальной жизни и способах борьбы с сексуальной дисфункцией на фоне лечения.
Важными компонентами такого комплексного лечения являются:
- консультирование у сексолога (психолога),
- использование вагинальных расширителей и увлажняющих кремов на фоне брахитерапии (не ранее чем через 4-6 недель после операции),
- медикаментозная терапия гипоактивного сексуального расстройства препаратами (Flibanserine (Addyi), Bremelanotide (Vyleesi), Bupropion).
“Hot issues in uterine tumors” (“Актуальные вопросы опухолей матки”), Frederic Amant, профессор, руководитель отделения онкогинекологии Лёвенского католического университета, Бельгия.
В рекомендациях Европейского общества онкогинекологов по лечению больных раком эндометрия в 2020 году появилась молекулярная классификация опухолей, играющая немаловажную, а порой и решающую роль при выборе тактики лечения.
Согласно этой классификации, выделяют 4 группы опухолей – с микросателлитной нестабильностью, pole мутированные, p53 и опухоли nsmp (не специфического молекулярного профиля).
Планирование послеоперационного лечения должно начинаться с анализа молекулярного профиля опухоли ввиду существенной разницы в прогнозах и чувствительности к различным модификациям терапии.
Так, например, от адъювантной химиотерапии выигрывают пациенты с мутацией р53.
В группе pole мутированных опухолей прогноз хороший даже без адъювантного лечения. Соответственно, у таких больных есть место для деэскалации лечения даже при второй стадии эндометриоидного рака. Опухоли с микросателлитной нестабильностью сравнительно плохо отвечают на химиотерапию, но являются чувствительными к иммунотерапии. Опухоли NSMP потенциально более чувствительны к химиотерапии, но имеют ряд других точек приложения.
MSI. Среди 39 типов солидных опухолей микросателлитная нестабильность встречается чаще всего именно при раке эндометрия, около 30%.
Частота ответов на иммунтерапию по результатам представленных исследований составила 45-57%.
Опухоли NSMP часто экспрессируют рецепторы эстрогена, прогестерона, а значит у таких пациентов есть место для гормонотерапии, которая является одной из основных опций лечения выскодиференцированного гормонпозитивного медленно прогрессирующего рака эндометрия.
“HPV vaccines. State of art” (“Вакцины от ВПЧ. Современное состояние проблемы”), Murat Gultekin, Профессор, Zekai Tahir Burak Maternity Hospital, Анкара, Турция.
Вирус папилломы человека является основным фактором риска развития рака шейки матки.
Мурат Гултекин рассказал о меняющейся тенденции в вакцинопрофилактике ВПЧ. Сегодня вакцинация показана мальчикам и девочкам с 9 лет. Не смотря на наличие рекомендаций о трехкратной вакцинации в возрасте 15-45 лет, ряд сообществ смещает фокус в сторону однократной иммунизации:
- Стратегическая консультативная группа экспертов ВОЗ (SAGE) по иммунизации - однократная вакцинация Гардасил-9 до 20 лет.
- Австралийская техническая консультативная группа по иммунизации (ATAGI) - однократная вакцинация Гардасил-9 до 20 лет.
- Международное агентство по изучению рака (IARC), Индия - однократная вакцинация Гардасил-9 до 18 лет.
Вакцинация также рекомендована людям, у которых уже диагностирован ВПЧ.
"Нерешенные вопросы неоадьювантной терапии при раке шейки матки", Носов Владимир Борисович, к.м.н., доцент кафедры акушерства, гинекологии и репродуктивной медицины МГМСУ, руководитель центра сохранения репродукции у онкологических пациентов, Европейский медицинский центр, Москва, Россия.
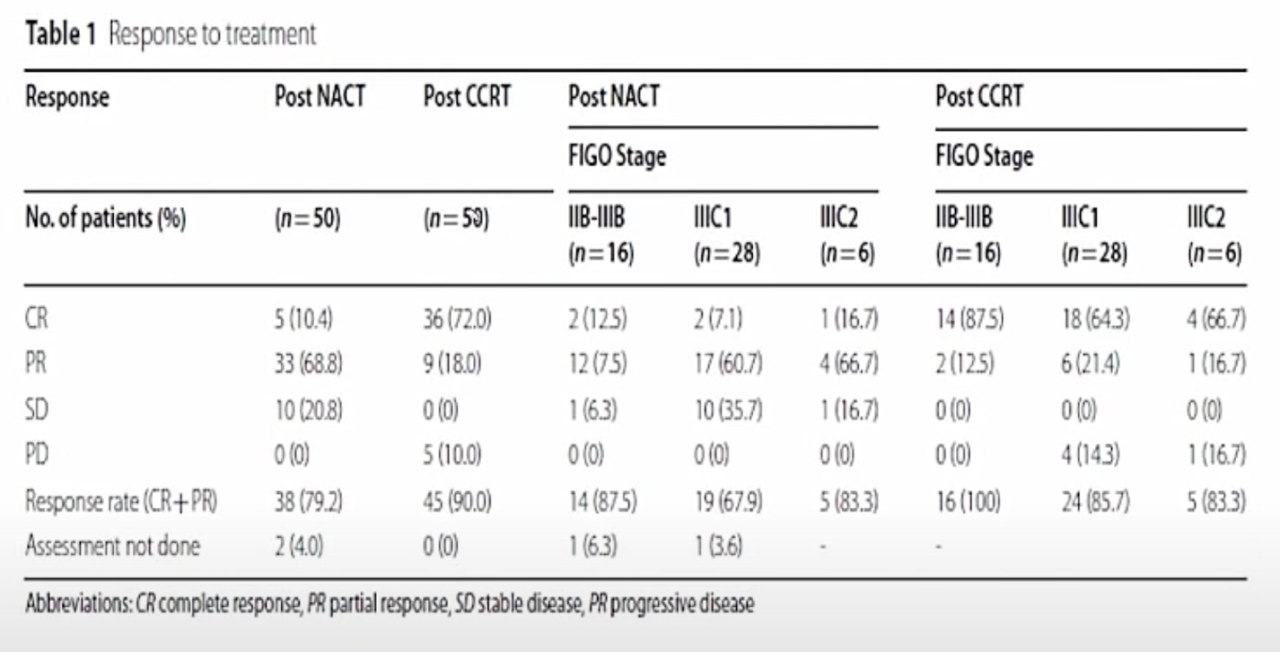
Неоадъювантная терапия (НАХТ) может быть рассмотрена в тех случаях, когда речь идет об органсохранном лечении у женщин с нереализованной репродуктивной функцией. Владимир Борисович привел результаты самого крупного по данному вопросу исследованию EORTC 55994.
Выводы:
- НАХТ не является стандартом лечения рака шейки матки, но допустима при стадиях 1В2-2В, если лучевая терапия недоступна.
- Нет данных о безопасности и эффективности НАХТ при стадиях III-IV.
- Репродуктивные планы + опухоль 2-4 см → НАХТ для уменьшения опухоли <2 см и последующей консервативной хирургией. Онкологические прогнозы существенно не отличаются.
- 1В3 - не кандидаты для НАХТ + консервативной хирургии.
"Challenging situation with cervical cancer" (“Непростая ситуация с раком шейки матки”), Татьяна Рабин, Руководитель центра лучевой терапии медицинского центра им. Х.Шиба, Тель-Авив, Израиль.
Татьяна Рабин рассказала о важности использования МРТ при планировании как дистанционной, так и брахитерапии и привела основные техники и нюансы дозирования лучевой нагрузки.
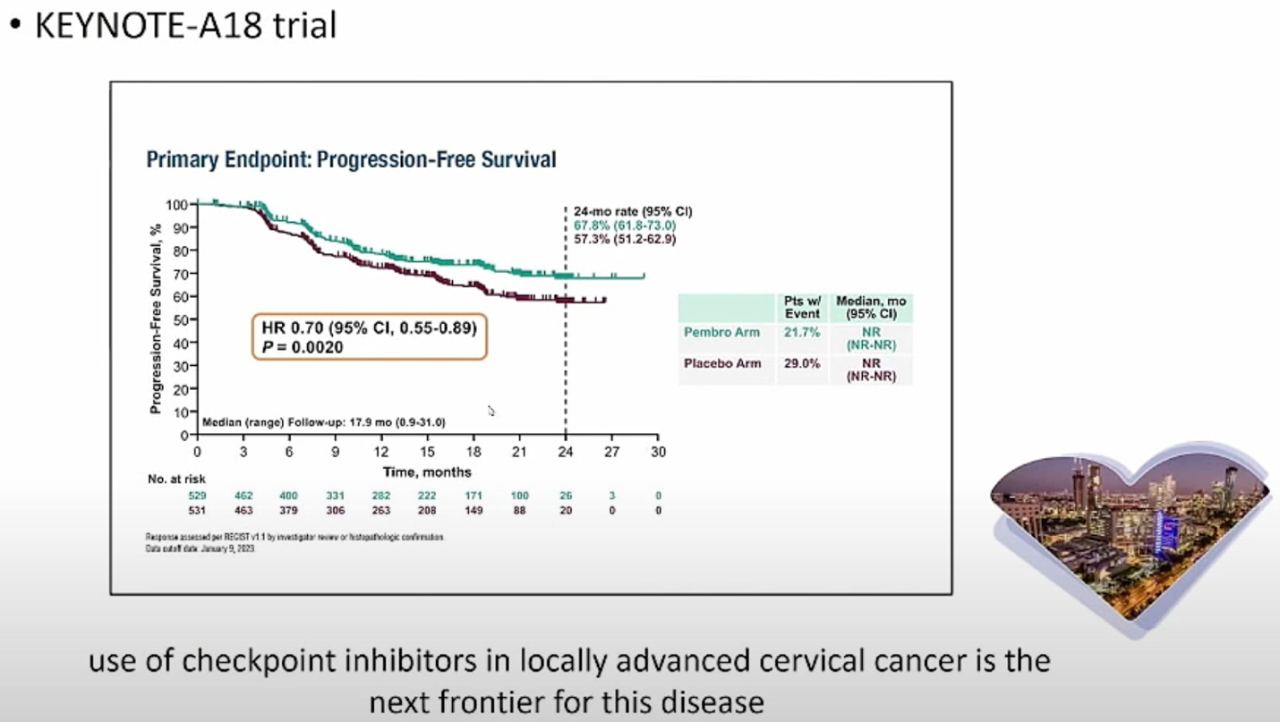
Обосновано изменение рекомендаций по лечению местнораспространенного рака шейки матки с добавлением 4 циклов неоадъювантной химиотерапии до начала лучевого лечения, а также использование ингибиторов контрольных точек в качестве одного из компонентов лекарственной неоадъювантной терапии.
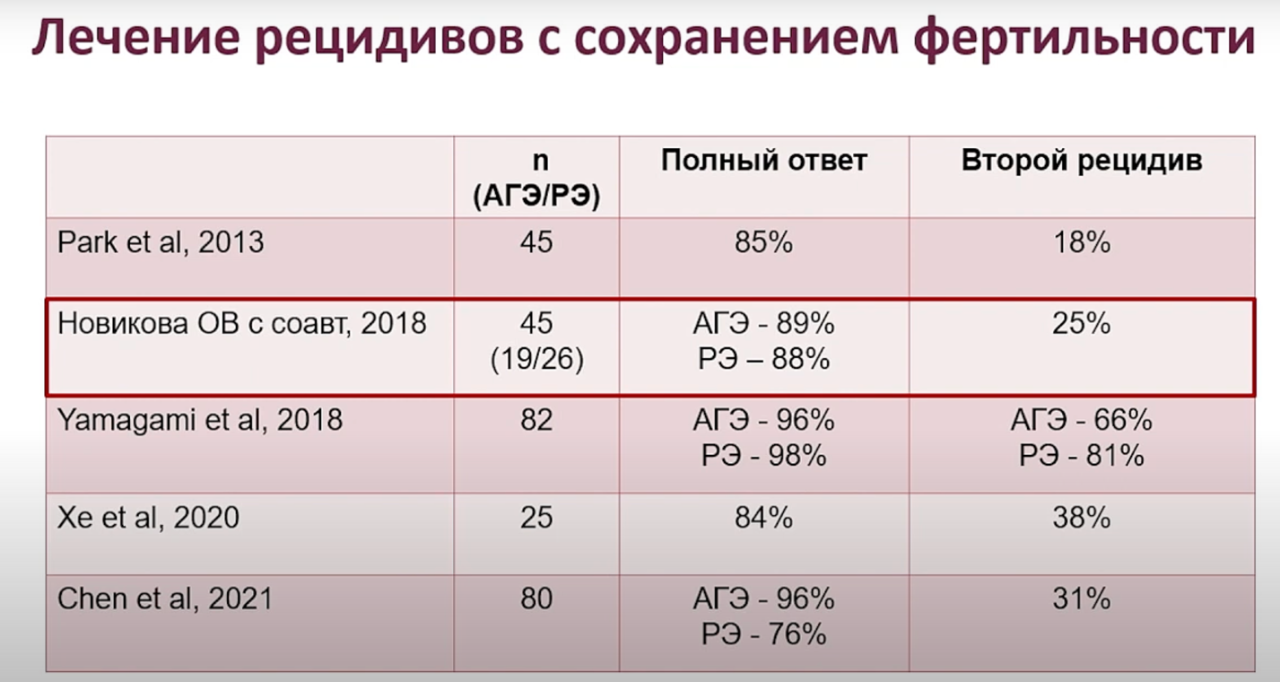
"Дискуссионные вопросы консервативного лечения начального рака эндометрия", Новикова Ольга Валерьевна, д.м.н., руководитель Центра лечения гинекологического рака, Клиника Фомина, Москва, Россия.
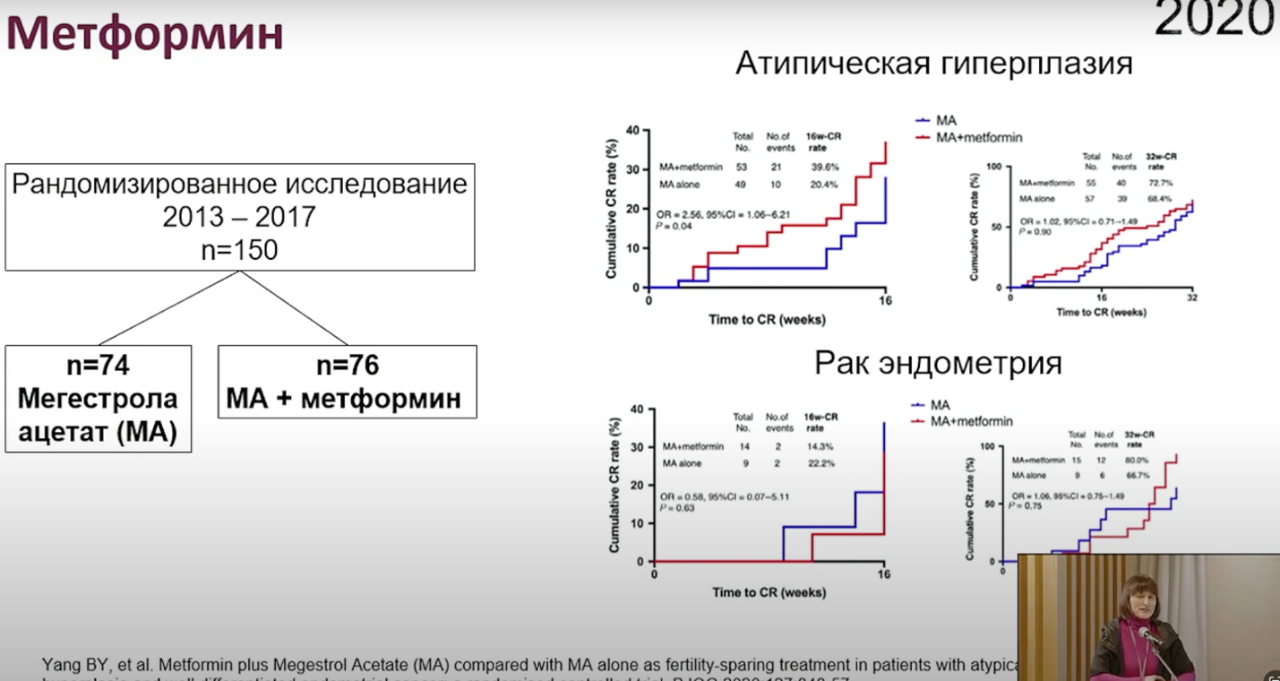
Гормональная терапия начального рака эндометрия показана пациентам, желающим сохранить репродуктивную функцию при эндометриоидном раке тела матки IA стадии G1. Наиболее спорными вопросами являются изменение критериев отбора пациенток для консервативного лечения, то есть расширение показаний и включение опухолей с умеренной дифференцировкой, а также лечение рецидивов с сохранением фертильности.
Добавление метформина у пациенток с ожирением улучшает прогнозы гормональной терапии.
Лечение умеренно дифференцированного рака не является стандартом, несет более высокие риски рецидива, но может быть рассмотрено в индивидуальных случаях.
Лечение рецидивов рака эндометрия гормонотерапией возможно, однако риск последующих рецидивов составляет 25%.
"Эндометриоз и рак. Есть ли связь?", Сонова Марина Мусабиевна, д.м.н. Ильинская больница, Москва, Россия.
Эндометриоз на сегодня остается одним из самых загадочных заболеваний 20-21 в. и рассматривается как гормонозависимое, генетически детерминированное заболевание, развивающееся на фоне нарушения иммунного гомеостаза. Его сущность заключается в разрастании ткани, идентичной по структуре и функции с эндометрием, но находящейся за пределами границ нормальной локализации слизистой оболочки тела матки. Частота этого заболевания у женщин репродуктивного возраста составляет около 10%. По данным различных авторов, эндометриоз встречается у 25-35% женщин с бесплодием и почти у 70% у женщин с тазовыми болями. Вопрос о возможности трансформации данного заболевания в злокачественные новообразования является очень важным, так как восприятие эндометриоза как заболевания без учета онкологического аспекта было бы неполным.
Впервые морфологическая взаимосвязь между эндометриозом и эндометриоидным раком яичников была выявлена J.A. Sampson в 1925 г. Опираясь на большой клинико-морфологический материал, Я.В. Бохман предположил, что последовательность событий при малигнизации эндометриоза отчетливо выступает лишь в ранней стадии развития рака, когда удается проследить всю «галерею структур» от эндометриоза до инвазивного эндометриоидного рака. При дальнейшем росте опухоль может полностью занять тот участок, где она возникла, и «поглотить» ткани, которые ей предшествовали. Возможно, поэтому есть затруднения в доказательстве этой связи.
Эндометриоз, оставаясь доброкачественным заболеванием, тем не менее обладает такой же способностью к пролиферации, инвазии, снижению апоптоза, неоангиогенезу, в редких случаях, но все же к метастазированию, что характерно для злокачественных заболеваний, в первую очередь, для рака яичников. Проблема рецидивов эндометриоза и его ассоциация с онкологической патологией является не решенной и по сей день. При развитии рака яичников у пациентов с эндометриозом чаще всего наблюдается его эндометриоидная форма в 40–55%, светлоклеточный рак — в 20–40%, серозные и муцинозные варианты рака выявляются намного реже, их не более 10%. Выводы о том, что эндометриоз ассоциируется со значительным ростом числа светлоклеточного и эндометриоидного рака яичников, являются стимулом для углубленного изучения этого вопроса и патогенеза эндометриоза в целом. Кроме того, эндометриоз ассоциируется с повышенным риском развития рака молочной железы, рака эндометрия и колоректального рака, что важно помнить всем врачам в обычной практике. Однако эти исследования продолжаются для определения тактики ведения этой категории пациенток в будущем. Несмотря на двукратное повышение риска развития рака яичников у категории пациентов с эндометриозом по сравнению с общей популяцией, пока не разработаны скрининговые программы. Однако понятно, что эта группа должна быть выделена в группу риска и требует индивидуального подхода.
Врач акушер-гинеколог, д.м.н., Сонова Марина Мусабиевна рассказала о состоянии проблемы на основе данных современной литературы, в том числе, ссылаясь на свои собственные публикации, посвященные проблеме возможной связи рака и эндометриоза.
"Is HIPEC a standard or an option in ovarian cancer?” (“Является ли HIPEC стандартом или опцией при лечении рака яичников?”), Elena Ratner. Профессор. Руководитель отделения онкогинекологии. Йельский университет. Нью-Хейвен, Коннектикут, США.
На сегодняшний день гипертермическая химиоперфузия не является признанным мировым стандартом для первичного лечения пациентов, страдающих раком яичников. Тем не менее, ее роль при хирургии рецидивов нельзя недооценивать. Единого мирового консенсуса по этому вопросу нет. Татьяна Ратнер поделилась алгоритмом отбора пациентов, которым пользуются онкогинекологи Йельского университета.














 Ильин Антон Алексеевич
Ильин Антон Алексеевич